http://www.asyura2.com/16/iryo5/msg/673.html
| Tweet |
アルツハイマー型認知症の治療薬が2020年に実用化!?
https://headlines.yahoo.co.jp/article?a=20171102-00000093-sasahi-hlth
AERA dot. 11/12(日) 7:00配信
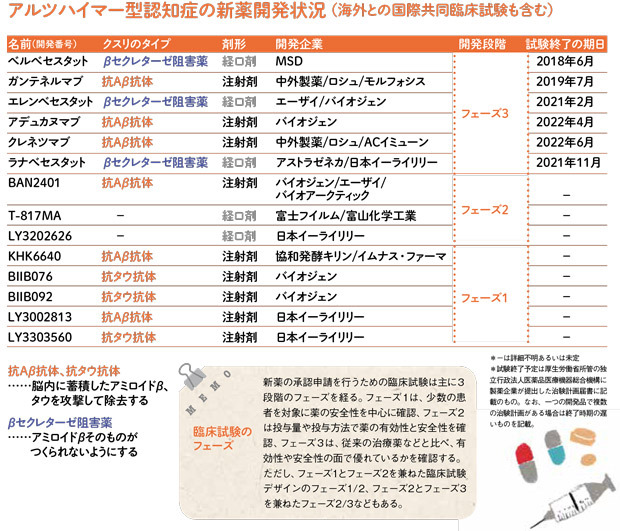
アルツハイマー型認知症の新薬開発状況
アルツハイマー型認知症の治療薬をつくるべく、各社が競って研究を進めている。週刊朝日MOOK「家族で読む予防と備え すべてがわかる認知症2017」では、研究の現場を取材した。
* * *
高齢化に伴い増加するアルツハイマー型認知症(以下、AD)に関しては現在、4種類の治療薬が存在する。しかし、日本では2011年7月を最後に、ADに対する新薬は登場していない。患者数が増加の一途をたどっている病気で、ここまで長期にわたって新薬が登場しないケースは珍しい。
この現象は日本特有のことではない。アメリカ研究製薬工業協会が15年7月に公表したAD治療薬の開発に関する報告書では、同協会会員の製薬企業が1998〜2014年に臨床試験をおこなったAD治療薬候補127成分のうち、製造承認に至ったのはたった4成分。確率にして3.1%だ。一般的に、薬の開発では臨床試験に入ったもののうち10%強が患者に投与されるところまで行きつく。つまり、これはかなり低い成功確率なのだ。
AD治療薬の開発の困難さに関して、昭和大学薬学部薬理学講座教授の野部浩司氏は、「ADはいまだ原因が明確ではないにもかかわらず、新たな物質(新薬)の効果を評価することが求められている難しい領域」と語る。簡単に言うなら、正体のわからない敵に効果のわからない手段で立ち向かうという状態なのだ。
その理由に迫る前に、そもそもADが起きる仕組みを説明したい。ADはアミロイドβ(以下、Aβ)、タウと呼ばれるたんぱく質が塊を形成して脳内に蓄積することで神経細胞が死滅し、記憶障害などの症状が出る。この過程で神経細胞が弱っていき、神経と神経の間で情報伝達を担う神経伝達物質の量も異常になり、記憶力の低下に拍車がかかるとされている。現在ある4種類の治療薬は、いずれも神経伝達物質の量を調整し、記憶力低下を回復させる。
■Aβとタウの蓄積を止める薬が必要
しかし、この回復は一時的。この間にもAβやタウの蓄積で神経細胞の死滅は進行していくので、これら治療薬で神経伝達物質の量を調整しても意味がなくなってしまうからだ。より根本的な治療を目指すならば、Aβやタウの蓄積を止める薬が必要になる。
実はこのAβとタウの蓄積は、ADの原因とは断定できていない。進行とともに患者の脳内に蓄積が進むため「原因だろう」と推定されている仮説なのだ。
Aβ仮説とは、こうだ。Aβのたんぱく質は3段階あり、酵素によって切り出されてできた最初のAβはモノマーと呼ばれ、これが複数絡み合ってオリゴマーになり、さらにそれらがプラークという塊を形成して脳内に張りつき、徐々に神経細胞を侵してADに至る。段階を経るごとにAβは毒性を増していく。
仮説とはいえ現時点で最有力であるため、現在のAD治療薬開発の主流は、Aβをターゲットにしたものに集中している。多くはAβを排除する抗体(抗Aβ抗体)を注射で投与し、Aβを取り除こうとしている。ただ、仮説ゆえに開発途中で数々の困難にも直面している。
実際、16年11月、AD治療薬を開発する関係者や患者を落胆させた出来事が起きた。米の大手製薬会社・イーライリリーが、臨床試験を実施していた「ソラネズマブ」という抗Aβ抗体について、医薬品としての承認申請を行わないと発表したのだ。早期認可が期待されていたが、最終段階の国際共同臨床試験・EXPEDITION3の結果、偽薬と比べ、明確な有効性の差が示せなかったからだ。
既に12年には米ファイザーの抗Aβ抗体・バピネオズマブも十分な有効性が示せずに開発中止に追い込まれており、一見するとAβ仮説に希望の光はないかのように見える。
ところが、別のところでは明るい兆しが見え始めている。ソラネズマブの承認申請の断念に先立つ16年9月、イギリスの有力科学誌「ネイチャー」に米バイオジェンが開発する抗Aβ抗体「アデュカヌマブ」が初期の試験で有効性を示したことが報告された。
この試験では放射性診断薬を用いた陽電子放射断層撮影法(PET)という画像診断で、アデュカヌマブを投与した患者の脳内ではAβ量が徐々に減少することが明らかになったのである。
しかも、CDR-SB(臨床的認知症重症度判定尺度)、MMSE(ミニメンタルステート検査)といった認知機能テストでも、偽薬を投与した群に比べて病状の悪化は少なかった。このまま試験がうまく進めば22年前後に実用化が見込める。
米バイオジェンの日本法人バイオジェン・ジャパンの社長で研究開発本部長も務める鳥居慎一氏は、「アデュカヌマブが持つ特性と臨床試験の手法が良好な成績の理由だろう」と説明する。
具体的に説明すると、アデュカヌマブは前述のAβで最も毒性が高いとされる脳内のプラークを標的にしている。また、従来の抗Aβ抗体の臨床試験では、ある程度症状が進行した患者を対象にしていたが、アデュカヌマブでは、軽度あるいはその直前の前駆期と呼ばれる超初期のAD患者を対象としたのだ。
前駆期と呼ばれる患者は、自覚症状が少なく、医療機関になかなか足を運ばないため、臨床試験に組み入れるのが難しい。実はソラネズマブが承認申請を断念したのも、この辺に大きな理由がある。米イーライリリーの日本法人・日本イーライリリー研究開発本部の中村智実氏は、「ソラネズマブは軽度ADの患者で臨床試験をおこなったが、この段階でも症状はある程度進行しているため、対象として的確ではなかったとの専門家の意見は多い」と語った。
また、ソラネズマブはAβの第1段階であるモノマーを標的としていた。初期に血中にあるモノマーを減らせば、脳内のAβが血中に出てきてバランスを保とうとし、結果として脳内のAβが減るという「シンク仮説」に基づいた薬剤だったからだ。しかし、想定したほど脳内のAβは減少しなかった。
とはいえ中村氏は、「少ないながらも効果は認められたので、ソラネズマブが完全に失敗したとは思っていない」と語る。現在、新薬の臨床試験は中断したが、国際的な官民共同試験が進行しており、そこで成功すれば、再び日の目を見る可能性もある。
この対照的な結果は、他社の抗Aβ抗体開発にも影響を及ぼしている。Aβのプラークを標的とする「ガンテネルマブ」、オリゴマーをメイン標的とする「クレネツマブ」という2種類の抗Aβ抗体を開発する中外製薬。同社はアデュカヌマブの試験結果を基に、いずれの薬剤でも臨床試験の投与量を増量して臨床試験を再設計する方針を固めた。中外製薬のプライマリーライフサイクルマネジメント部の中谷紀章氏は、「Aβのなかでオリゴマー、プラークのどちらがADの主犯格かはまだわからない。今後われわれや各社の臨床試験の結果で、こうしたAβ仮説のさまざまな疑問が明らかになる」との見通しを示す。
■AD克服へ 各社の挑戦は続く
アリセプトを開発したエーザイは新たに、抗Aβ抗体の「BAN2401」とβセクレターゼ(BACE)阻害薬の「エレンベセスタット」を開発中だ。BACEはある種のたんぱく質からAβのモノマーを切り出す働きをする酵素。BACE阻害薬はいわばAβの源流を断つ戦略だ。後者は全世界で合計2660人の患者を集め、二つの臨床試験を実施している。
各社とも互いを横目で眺めながら、まさにトライアル・アンド・エラーの連続で治療薬の開発を進めている。これらのうち最も早く患者に届くものは、うまくいけば20年前後に登場する見込みだ。
ただ、現在開発中のAβターゲットの治療薬はADの進行を遅らせる薬で、完全に治せるものではない。しかし、これは必ずしも暗いニュースではない。そもそもADの発症は60〜70代に多い。今後登場する複数の薬でこれを10〜15年遅らせることができれば、天寿にほぼ近づき、事実上のAD克服といえるからだ。
(取材・文/村上和巳)
※週刊朝日MOOK「家族で読む予防と備え すべてがわかる認知症2017」
投稿コメント全ログ コメント即時配信 スレ建て依頼 削除コメント確認方法
 スパムメールの中から見つけ出すためにメールのタイトルには必ず「阿修羅さんへ」と記述してください。
スパムメールの中から見つけ出すためにメールのタイトルには必ず「阿修羅さんへ」と記述してください。すべてのページの引用、転載、リンクを許可します。確認メールは不要です。引用元リンクを表示してください。