http://www.asyura2.com/15/nature6/msg/147.html
| Tweet | پ@ |
پu‚ھ‚ٌ—}گ§چy‘f‚ً‰َ‚·‚±‚ئ‚جƒٹƒXƒNپvپi‚d‚i‘و‚S‚P‚O‚Xچ†پj
http://electronic-journal.seesaa.net/article/425054208.html
2015”N08Œژ31“ْپ@Electronic Journal
پ@“¯‚¶چؤگ¶ˆم—أ‚إ‚à‚‰‚o‚rچ×–E‚حƒmپ[ƒxƒ‹ڈـ‚ًژو‚èپA‚r‚s‚`‚oچ×
–E‚حƒCƒ“ƒ`ƒLŒ¤‹†‚ئ‚µ‚ؤ‘’‚è‹ژ‚ç‚ê‚é„ں„ں‚à‚µپA‚r‚s‚`‚oچ×–E‚ً
’ׂµ‚½گ¨—ح‚ًƒrƒbƒOƒtƒ@پ[ƒ}‚إ‚ ‚é‚ئ‰¼’肵‚½ڈêچ‡پA‚‰‚o‚rچ×–E
‚ح‚ب‚؛‹–‚³‚ê‚é‚ج‚©‚ة‚آ‚¢‚ؤپA’ا‹y‚µ‚ؤ‚¢‚ـ‚·پB
پ@‚»‚ج——R‚حٹب’P‚ب‚±‚ئ‚إ‚·پB‚‰‚o‚rچ×–E‚ًچؤگ¶ˆم—أ‚ةژg‚¤ڈêچ‡
‚³‚ـ‚´‚ـ‚ب‹ا–ت‚إچ‚‰؟‚ب–ٍ‚ًژg‚¤‚±‚ئ‚ھ•s‰آŒ‡‚إ‚ ‚é‚ج‚ة‘خ‚µ‚ؤ
‚r‚s‚`‚oچ×–E‚إ‚ح‚»‚ê‚ç‚ح‚ظ‚ئ‚ٌ‚ا•s—v‚ة‚ب‚é‚©‚ç‚إ‚·پB‚à‚µپA
‚r‚s‚`‚oچ×–E‚ھٹJ”‚³‚ê‚é‚ئپAƒrƒbƒOƒtƒ@پ[ƒ}‚ح‘ه‘إŒ‚‚ً”ي‚邱
‚ئ‚ة‚ب‚è‚ـ‚·پB‚»‚¤‚إ‚ ‚ê‚خپA‚»‚¤‚¢‚¤Œ¤‹†‚حƒ}ƒEƒX‚جŒ¤‹†‚ج’i
ٹK‚إ’ׂµ‚ؤ‚¨‚‚ج‚ھچإ‚àˆہ‘S‚ئ‚¢‚¤‚±‚ئ‚ة‚ب‚è‚ـ‚·پB
پ@ژR’†ƒtƒ@ƒNƒ^پ[‚ئŒؤ‚خ‚ê‚é‚S‚آ‚جˆâ“`ژq‚ج‚¤‚؟پu‚ƒ„ں‚l‚™‚ƒپv
پiپuƒVپ[پEƒ~ƒbƒNپv‚ئŒؤڈجپj‚حپA‚ھ‚ٌˆâ“`ژq‚ئ‚³‚ê‚ؤ‚¢‚ـ‚·پB’ت
ڈي‚حچ×–E‚ج‘گB‚ًگ§Œن‚·‚é“‚«‚ً‚µ‚ـ‚·‚ھپA‚±‚ê‚ھ‹‚“‚‚ئچ×
–E‚ً‚ھ‚ٌ‰»‚³‚¹‚邱‚ئ‚ة‚ب‚é‰آ”\گ«‚ھ‚ ‚è‚ـ‚·پB
پ@‚ب‚¨پA‚±‚ê‚ة‚آ‚¢‚ؤ‚حٹù‚ةڈq‚ׂؤ‚¢‚é‚و‚¤‚ةپAژR’†Œ¤‹†ژ؛‚إ‚ح
‚ƒ„ں‚l‚™‚ƒ‚ًژg‚ي‚ب‚¢‚إ‚àپA‚‰‚o‚rچ×–E‚ًچىگ»‚·‚邱‚ئ‚ةگ¬Œ÷‚µ
‚ؤ‚¢‚ـ‚·پBƒپƒfƒBƒA‚ح‚±‚ج‚±‚ئ‚ًپu‚‰‚o‚rچ×–E‚ًژg‚¤چؤگ¶ˆم—أ‚ة
‚¨‚¯‚é‚ھ‚ٌ‰»‚جƒٹƒXƒN‚حڈء–إپv‚ئ‚¢‚¤‚و‚¤‚ة•ٌ“¹‚µ‚ؤ‚¢‚ـ‚·‚ھپA
‚»‚ê‚حژ–ژہ‚ئˆظ‚ب‚è‚ـ‚·پB‚ھ‚ٌ‰»‚جƒٹƒXƒN‚ح‚؛‚ٌ‚؛‚ٌ‚ب‚‚ب‚ء‚ؤ
‚¢‚ب‚¢‚©‚ç‚إ‚·پB
پ@گl‘ج‚ح–ٌ‚U‚O’›Œآ‚ج‘جچ×–E‚©‚çچ\گ¬‚³‚ê‚ؤ‚¢‚ـ‚·پB‚±‚ê‚ç‚ج‘ج
چ×–E‚ة‚ح‚»‚ꂼ‚êژُ–½‚ھ‚ ‚èپA‚ ‚郌ƒxƒ‹‚ـ‚إ‘گB‚·‚é‚ئ‘گB‚ھ
ƒXƒgƒbƒv‚µپAپuڈIژnٹْپv‚ئ‚¢‚¤ڈI––ƒTƒCƒNƒ‹‚ة“ü‚è‚ـ‚·پB‚±‚ج‚ئ
‚«پA‚³‚ç‚ة‘گB‚µ‚و‚¤‚ئ‚·‚éچ×–E‚ةƒuƒŒپ[ƒL‚ً‚©‚¯‚éژں‚ج‚Qژي—ق
‚جچy‘f‚ھ‚ ‚è‚ـ‚·پB
„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں
پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@‚PپDپ@‚q‚a
پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@‚QپD‚o‚T‚R
„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں
پ@‚±‚ê‚ç‚Q‚آ‚جچy‘f‚ة‚و‚èپAŒأ‚¢چ×–E‚حگV‚µ‚¢چ×–E‚ة‘گB‚ًˆّ‚«
Œp‚®‚ج‚إ‚·پB‚±‚جƒTƒCƒNƒ‹‚ًپuƒZƒ‹ƒTƒCƒNƒ‹پv‚ئ‚¢‚¢‚ـ‚·پB‚±‚ج
چ×–E‚جگV‹ŒŒً‘م‚ًچs‚ي‚¹‚é‚ج‚ھپu‚q‚aپv‚ئپu‚o‚T‚Rپv‚ئ‚¢‚¤چy‘f
‚ب‚ج‚إ‚·پB‚±‚ج‚Q‚آ‚ھ‚ب‚¢‚ئپAƒZƒ‹ƒTƒCƒNƒ‹‚حگ³ڈي‚ة‰ٌ“]‚µ‚ب‚¢
‚±‚ئ‚ة‚ب‚è‚ـ‚·پB
پ@‚±‚ê‚çپu‚q‚aپv‚ئپu‚o‚T‚Rپv‚حپA‚ھ‚ٌ—}گ§چy‘f‚ئŒؤ‚خ‚êپA‚ھ‚ٌ
‰»‚µ‚و‚¤‚ئ‚·‚éچ×–E‚ة‚àƒuƒŒپ[ƒL‚ً‚©‚¯پA‚ھ‚ٌچ×–E‚ج‘گB‚ًژ~‚ك
‚é‹@”\‚ًژ‚ء‚ؤ‚¢‚é‚ج‚إ‚·پB
پ@‚µ‚©‚µپA‚‰‚o‚rچ×–E‚ً‘گB‚³‚¹‚و‚¤‚ئ‚·‚é‚ئپAپu‚q‚aپv‚ئپu‚o
‚T‚Rپv‚جƒuƒŒپ[ƒL‹@”\‚ھژ×–‚‚ة‚ب‚è‚ـ‚·پB‚‰‚o‚rچ×–E‚ج‘گB‚ًژ~
‚ك‚ؤ‚µ‚ـ‚¤‚©‚ç‚إ‚·پB‚»‚ج‚½‚كپA‚‰‚o‚rچ×–E‚ًچؤگ¶ˆم—أ‚ةژg‚¤‚ة
‚حپA‚ ‚ç‚©‚¶‚كپAپu‚q‚aپv‚ئپu‚o‚T‚Rپv‚ئ‚¢‚¤‚Q‚آ‚جچy‘f‚ً‰َ‚µ
‚ؤ‚µ‚ـ‚¤‚ج‚إ‚·پB
پ@‚±‚ê‚ةٹض‚µ‚ؤŒxڈà‚ً–آ‚炵‚ؤ‚¢‚é‚ج‚ھٹùڈo‚ج’O‰HچkژOˆمژt‚ب‚ج
‚إ‚·‚ھپAŒ¤‹†ژز‚àƒپƒfƒBƒA‚à‚±‚ê‚ً–ظژE‚µ‚ؤ‚¢‚ـ‚·پB‚±‚ê‚ةٹض‚·
‚é’O‰HچkژOˆمژt‚جچl‚¦•û‚ًنtگ£ڈr‰îژپ‚ج–{‚©‚çˆّ—p‚µ‚ـ‚·پB
„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں
پ@پuچؤگ¶ˆم—أ‚ج‚‰‚o‚rچ×–E‚إ‚حپA‚ ‚éچ×–E‚ً‚ا‚ٌ‚ا‚ٌ‘گB‚³‚¹‚و
‚¤‚ئ‚µ‚ـ‚·پB‚آ‚ـ‚èپi‚‰‚o‚rچ×–E‚حپjˆê”شٹî–{“I‚بپwچ×–Eژüٹْپx
‚إ‚ ‚éپwڈIژnٹْپx‚ة“ü‚ء‚ؤ‚حپA‚¢‚¯‚ب‚¢‚ج‚إ‚·پvپi’O‰Hˆمژtپj
پ@‚آ‚ـ‚èپA‚‰‚o‚rچؤگ¶ˆم—أ‚إ‚حپA‘ه—ت‚ج‚‰‚o‚rچ×–E‘gگD‚ً•K—v‚ئ
‚·‚éپB‚µ‚©‚µپAگ¶–½‚ة‚حپuچ×–Eژüٹْپv‚ھ”ُ‚ي‚ء‚ؤ‚¢‚éپB‚»‚ج‚½‚ك
‚ةپA‚Q‚آ‚ج‘گB—}گ§چy‘fپiƒuƒŒپ[ƒLپj‚ھ‘¶چف‚·‚éپB‚µ‚½‚ھ‚ء‚ؤپA
‚‰‚o‚rچ×–E‚ًچى‚é‚ئ‚«‚ة‚حپAپu‚q‚aپvپu‚o‚T‚Rپvچy‘f‚ھژ×–‚‚ة‚ب
‚éپB‚»‚±‚إپA‚‰‚o‚rچ×–E‚ًچىگ¬‚·‚éژ‚ة‚حپA—¼چy‘f‚ج“‚«‚ًپu’@
‚¢‚ؤٹ®‘S‚ةƒXƒgƒbƒv‚³‚¹‚ؤ‚¢‚éپv‚ئ’O‰Hˆمژt‚حژw“E‚·‚éپB
پ@‚ب‚؛‚ب‚çپA‚‰‚o‚rچ×–E‚ًچؤگ¶ˆم—أ‚ة—p‚¢‚邽‚ك‚ة‚حپAچ×–E‘گB
‚³‚¹‚é•K—v‚ھ‚ ‚éپBڈ‚ب‚‚ئ‚à‘gگDƒŒƒxƒ‹‚ة‚ـ‚إگ¬’·‚³‚¹‚ب‚¯‚ê
‚خ‚ب‚ç‚ب‚¢پB‚»‚ê‚ة‚حپAƒZƒ‹ƒTƒCƒNƒ‹پuڈIژnٹْپv‚ة“ü‚ء‚½‚ئ‚«پA
پu‚q‚aپvپu‚o‚T‚Rپv—¼ƒuƒŒپ[ƒLچy‘f‚ھژ×–‚‚ة‚ب‚éپB‚»‚±‚إƒuƒŒپ[
ƒL‚ً”j‰َ‚·‚éپB‚±‚ê‚ھ‚‰‚o‚rچ×–EٹJ”‚جٹî–{ƒeƒNƒjƒbƒN‚ب‚ج‚¾پB
پ@’O‰Hˆمژt‚حپAڈd‘ه‹^کf‚ً“ٹ‚°‚©‚¯‚éپBپu‚±‚ج‚±‚ئ‚ة‚‰‚o‚rچ×–E
‚جŒ¤‹†ژز‚½‚؟‚حپAˆêŒ¾‚àگG‚ê‚ؤ‚¨‚è‚ـ‚¹‚ٌپB‚±‚جˆظڈي‘گB‚ً—}‚¦
‚é‚q‚aپA‚o‚T‚R‚ً’@‚‚ئپAƒKƒ“‰»‚ة‚ب‚è‚©‚¯‚ؤ‚¢‚½چ×–E‚ھپA‚ا‚ٌ
‚ا‚ٌ‘ه‚«‚‚ب‚ء‚ؤƒKƒ“‰»‚µ‚ـ‚·پvپBپ@پ@پ@پ@پ@پ@„ں„ں‘Dگ£ڈr‰î’ک
پ@پ@پ@پ@پ@پ@پ@پ@پw‚r‚s‚`‚oچ×–E‚جگ³‘جپ^پuچؤگ¶ˆم—أ‚حŒ¶‘z‚¾پv
پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@•œٹˆپIگ瓇پEگX‰؛ٹwگàپxپ^‰ش“`ژذٹ§
„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں
پ@ƒچƒbƒNƒtƒFƒ‰پ[‚ھ‚»‚¤‚إ‚ ‚é‚و‚¤‚ةپAŒ —حژز‚حƒپƒfƒBƒA‚ً‚ـ‚¸
ٹ®‘S‚ةژx”z‚µ‚ـ‚·پBƒپƒfƒBƒA‚ھ’¾–ظ‚·‚é‚ئپA‚±‚¤‚¢‚¤‘fگl‚ة‚ح‚ي
‚©‚è‚ة‚‚¢ڈî•ٌ‚ح“`‚ي‚è‚ة‚‚‚ب‚è‚ـ‚·پB
پ@‚»‚±‚إپA’O‰HچkژOˆمژt‚حپAپuچؤگ¶ˆم—أپvŒ¤‹†ƒOƒ‹پ[ƒv‚ة‘خ‚µ‚ؤ
‚Q‚O‚P‚Q”N‚ج‚ح‚¶‚ك‚ةژں‚جŒِٹJژ؟–âڈَ‚ً‘—‚ء‚ؤ‚¢‚ـ‚·پB
„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں
پ@‚‰‚o‚rچ×–E‚ًچىگ¬‚·‚邳‚¢پA‚o‚T‚R‚ج“]ژت”\—ح‚ھ•sٹˆگ«‰»‚³‚ê
‚ؤ‚¢‚ب‚¢پi‚o‚T‚R‚جچ×–E‘گB—}گ§چى—p‚ھˆغژ‚³‚ê‚ؤ‚¢‚éپjƒ~ƒgƒR
ƒ“ƒhƒٹƒA‚ب‚ا‚إپAژہچغپA‚ا‚¤‚â‚ء‚ؤپA‚o‚T‚R‚â‚q‚a‚½‚ٌ‚د‚‚ً—}
‚¦‚é‘€چى‚ً‚µ‚ؤ‚‰‚o‚rچ×–E‚ً‘‚₵‚ؤ‚¨‚ç‚ê‚é‚©پB„ں„ں’O‰HچkژO
پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@„ں„ں‘Dگ£ڈr‰î’ک‚ج‘OŒfڈ‘‚و‚è
„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں
پ@Œ¤‹†ƒOƒ‹پ[ƒv‚©‚ç‚ج‰ٌ“ڑڈ‘‚ح’O‰Hˆمژt‚ة“ح‚¢‚½‚ج‚إ‚·‚ھپA“à—e
‚حˆê”تک_‚ةڈIژn‚µپA—v‚·‚é‚ة‰½‚à“ڑ‚¦‚ؤ‚¢‚ب‚©‚ء‚½‚»‚¤‚إ‚·پB’O
‰Hژپ‚جژw“E‚µ‚ؤ‚¢‚邱‚ئ‚حژ–ژہ‚إ‚ ‚èپA‚ـ‚ئ‚à‚ة“ڑ‚¦‚邱‚ئ‚ح‚إ
‚«‚ب‚©‚ء‚½‚ج‚إ‚·پB
پ@ژہ‚ح–ٌ‚Q‚O”N‘OپA‚q‚aپA‚o‚T‚R‚ة‚آ‚¢‚ؤ‚ح‘½‚‚جٹwژز‚ھŒ¤‹†‚µ
‚ؤ‚¨‚èپAک_•¶‚à‘½گ”‚ ‚é‚ج‚إ‚·پB‚»‚±‚إ‚حپA‚±‚ê‚ç‚q‚aپA‚o‚T‚R
‚ھ‘ج“à‚إ‚¢‚©‚ة•K—v‚بچy‘f‚إ‚ ‚é‚©پAک_‚¶‚ç‚ê‚ؤ‚¢‚é‚ج‚إ‚·پB
پ@‚µ‚©‚é‚ةپA‚‰‚o‚rچ×–E‚ھگ¢‚ةڈo‚ؤ‚©‚ç‚ئ‚¢‚¤‚à‚جپA‚±‚ê‚ç‚جچy
‘f‚ةٹض‚µ‚ؤ‚حپA’N‚àگG‚ê‚و‚¤‚ئ‚ح‚µ‚ب‚¢‚ج‚إ‚·پB‚ھ‚ٌ—}گ§چy‘f‚ً
‰َ‚¹‚خپA‚ھ‚ٌ‚ة‚ب‚éƒٹƒXƒN‚ح‘fگl‚إ‚à‚ي‚©‚é‚©‚ç‚إ‚·پB
پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@پ@„ں„ں پm‚r‚s‚`‚oچ×–Eژ–Œڈپ^‚O‚W‚Qپn
پل‰و‘œ‚¨‚و‚رٹضکAڈî•ٌپâ
پ@پœ‚‰‚o‚rچ×–E‚ئ‚ھ‚ٌ—}گ§ˆâ“`ژq‚ئ‚جٹضŒWپ^‚Q‚O‚O‚X”N‚WŒژ
پ@پ@„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں
پ@پ@پ@‚o‚T‚R‚حپCژîل‡‚ج”گ¶‚ً—}‚¦‚é“‚«‚ج‚ ‚éڈd—v‚بٹà—}گ§ˆâ
پ@پ@“`ژq‚إپuƒQƒmƒ€‚جژçŒىگ_پv‚ئ‚جˆظ–¼‚ً‚à‚؟پA–{ˆâ“`ژq‚جˆظڈي
پ@پ@‚حپCٹàچ×–E‚ة‚¨‚¢‚ؤچ‚—¦‚ة”Œ©‚³‚ê‚ؤ‚¢‚éپB‚Q‚O‚O‚U”N‚ةژR
پ@پ@’†گL–ي‹³ژِپi‹“s‘هٹwپj‚ç‚حپC‚Rپ`‚S‚آ‚جˆâ“`ژq‚ة‚و‚ء‚ؤپA
پ@پ@‘جچ×–E‚©‚炉‚o‚rچ×–E‚ئ‚¢‚¤گlچH“I‚ب‘½”\گ«ٹ²چ×–Eپi–œ”\چ×
پ@پ@–Eپj‚ًچى‚èڈo‚·‚±‚ئ‚ةگ¬Œ÷‚µ‚½پB‚±‚ج‚‰‚o‚rچ×–E‚جچىگ¬‚ج‰ك
پ@پ@’ِ‚حپuچؤƒvƒچƒOƒ‰ƒ~ƒ“ƒO(ڈ‰ٹْ‰»)پv‚ئŒؤ‚خ‚ê‚é‚ھپAژہچغ‚ة‘ج
پ@پ@چ×–E‚ھڈ‰ٹْ‰»‚³‚ꂉ‚o‚rچ×–E‚ة‚ب‚éٹm—¦‚ح”ٌڈي‚ة’ل‚¢پB
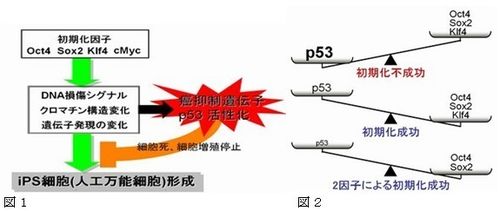
پ@پ@پ@چ،‰ٌ‚جŒ¤‹†گ¬‰ت‚ة‚و‚èپA‚±‚جپuچؤƒvƒچƒOƒ‰ƒ~ƒ“ƒOپv‚ً‚o‚T
پ@پ@‚R‚ھ—}گ§‚µ‚ؤ‚¢‚½‚±‚ئ‚ھ–¾‚ç‚©‚ة‚ب‚ء‚½(گ}‚P)پB‚o‚T‚R‚ج‹@
پ@پ@”\‚ً’ل‰؛‚³‚¹‚½ƒqƒg‚âƒ}ƒEƒX‚جچ×–E‚ً—p‚¢‚é‚ئپAچ‚—¦‚إ‚‰‚o
پ@پ@‚rچ×–E‚ًچىگ»‚·‚邱‚ئ‚ھ‚إ‚«‚½(گ}‚Q)پB‚³‚ç‚ة‚o‚T‚R‚ج‹@”\
پ@پ@‚ھ’ل‰؛‚µ‚½چ×–E‚حپC“–ڈ‰ژR’†‹³ژِ‚ç‚ھ‚‰‚o‚rچ×–E‚جچىگ»‚ة•K
پ@پ@—v‚ئ”•\‚µ‚½‚Sˆِژq‚ج‚¤‚؟‚Q‚آ‚ً‰ء‚¦‚邾‚¯‚إ‚‰‚o‚rچ×–E‚ة
پ@پ@‚ب‚邱‚ئ‚ھ‚إ‚«‚½(گ}‚Q)پBڈ‰ٹْ‰»‚ً‘£‚·‚±‚ئ‚ة‚و‚èپA‘جچ×–E
پ@پ@‚ج‚ب‚©‚إ‚حپAٹà—}گ§ˆâ“`ژq‚o‚T‚R‚ھٹˆگ«‰»‚³‚êپA‚‰‚o‚rچ×–E
پ@پ@Œ`گ¬‚ھ‹—ح‚ة—}‚¦‚ç‚ê‚ؤ‚¢‚é‚ئچl‚¦‚ç‚ꂽ(گ}‚P)پB‚‰‚o‚rچ×
پ@پ@–E‚جچىگ¬‚ئ”ٹà‚ئ‚جٹش‚ة‰½‚ç‚©‚جٹض‚ي‚è‚ھ‚ ‚邱‚ئ‚ھگ„‘ھ‚³
پ@پ@‚ê‚éپB‚±‚ج‚و‚¤‚ةپA–{Œ¤‹†‚ح–¢‰ً–¾‚بپuچؤƒvƒچƒOƒ‰ƒ~ƒ“ƒOپv
پ@پ@‚جژd‘g‚ف‚جˆê’[‚ً–¾‚ç‚©‚ة‚µپAڈ«—ˆ‚ج‚‰‚o‚rچ×–E‚ج—صڈ°‰—p
پ@پ@‚ةŒü‚¯‚½‚و‚èˆہ‘S‚©‚آٹب•ض‚إŒّ—¦“I‚ب‚‰‚o‚rچ×–Eچىگ¬–@‚جٹm
پ@پ@—§‚ة–ً—§‚آ‚à‚ج‚ئچl‚¦‚ç‚ê‚éپBپ@پ@ http://bit.ly/1Vn3JDD
پ@پ@„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں„ں
پ@
|
|
|
|
“ٹچeƒRƒپƒ“ƒg‘SƒچƒO پ@ƒRƒپƒ“ƒg‘¦ژ”zگM پ@ƒXƒŒŒڑ‚ؤˆث—ٹ پ@چيڈœƒRƒپƒ“ƒgٹm”F•û–@
پ£ڈم‚ضپ@پ@پ@پ@پ@ پڑˆ¢ڈC—…پô > ٹآ‹«پEژ©‘RپE“V•¶”آ6Œfژ¦”آپ@ژں‚ض پ@‘O‚ض
|
|
 ƒXƒpƒ€ƒپپ[ƒ‹‚ج’†‚©‚猩‚آ‚¯ڈo‚·‚½‚ك‚ةƒپپ[ƒ‹‚جƒ^ƒCƒgƒ‹‚ة‚ح•K‚¸پuˆ¢ڈC—…‚³‚ٌ‚ضپv‚ئ‹Lڈq‚µ‚ؤ‚‚¾‚³‚¢پB
ƒXƒpƒ€ƒپپ[ƒ‹‚ج’†‚©‚猩‚آ‚¯ڈo‚·‚½‚ك‚ةƒپپ[ƒ‹‚جƒ^ƒCƒgƒ‹‚ة‚ح•K‚¸پuˆ¢ڈC—…‚³‚ٌ‚ضپv‚ئ‹Lڈq‚µ‚ؤ‚‚¾‚³‚¢پB‚·‚ׂؤ‚جƒyپ[ƒW‚جˆّ—pپA“]چعپAƒٹƒ“ƒN‚ً‹–‰آ‚µ‚ـ‚·پBٹm”Fƒپپ[ƒ‹‚ح•s—v‚إ‚·پBˆّ—pŒ³ƒٹƒ“ƒN‚ً•\ژ¦‚µ‚ؤ‚‚¾‚³‚¢پB