http://www.asyura2.com/09/iryo03/msg/868.html
| Tweet |

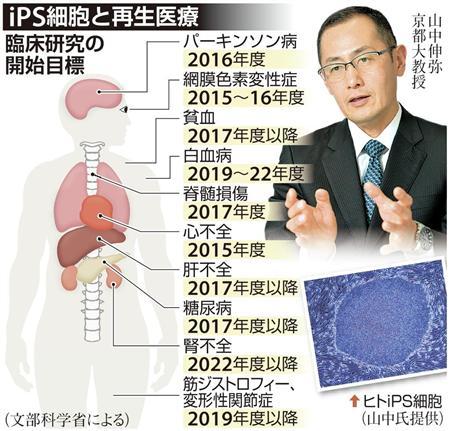
「理研STAP」騒動横目に…「京大iPS」パーキンソン病治療へ着々
http://headlines.yahoo.co.jp/hl?a=20140416-00000516-san-sctch
産経新聞 4月16日(水)12時20分配信
新型万能細胞「STAP細胞」の論文を巡る問題が泥沼化するなか、人工多能性幹細胞(iPS細胞)の生みの親、山中伸弥教授が所長を務める京都大iPS細胞研究所(CiRA=サイラ=)が、いよいよ再生医療の臨床研究に向かって動き出した。iPS細胞を使ったパーキンソン病の治療を目指すCiRAの高橋淳教授らのグループは、ヒトのiPS細胞から神経細胞を作製する際に余分な細胞が混入しないよう選別するなど、安全で効率的な培養技術を確立。臨床研究で用いる手法が、ほぼ固まった。STAP細胞の発表当初、とかく比較されたiPS細胞だったが、着々と臨床に向かっている。来年1月にも臨床研究を申請し、実際に手術を行うのは平成28年ごろになるという。
■網膜に続き2例目
パーキンソン病は、脳内で情報を伝える物質のドーパミンが少なくなり、運動などに支障が生じる難病。国内に約14万人の患者がいるが、根本的な治療法はないとされる。高橋教授は、iPS細胞からドーパミンを出す神経細胞を作って患者の脳に移植する再生医療を目指しており、「10年以内には実用化して、一般の患者が治療を受けられるようにしたい」と話す。
高橋教授らは、昨年11月に成立した再生医療安全性確保法に基づいて京都大に設置される「特定認定委員会」に対し、来年1月にも臨床研究を申請する。
ここで了承を得れば、厚生労働省による安全性の確認を経て、来年中に臨床研究をスタート。京大付属病院などの患者から6人前後を選び、血液細胞から作製したiPS細胞を神経細胞に分化させる。さらに安全性の検証などを行った上で、数千万個の神経細胞を患者の脳に移植する。
iPS細胞を使った臨床研究としては、高橋教授の妻でもある理化学研究所発生・再生科学総合研究センター(神戸市)の高橋政代プロジェクトリーダーらが取り組んでいる網膜の再生による目の難病「加齢黄斑変性」の治療に続き、世界で2例目となる見通しだ。
■安全な手法を確立
臨床研究に向け、高橋教授らはiPS細胞から大量の神経細胞を作製する技術と、余分な細胞が混入しないように選別する技術を確立した。
iPS細胞による再生医療では、目的の細胞を大量に用意する必要がある。従来、iPS細胞などの培養には動物由来成分を含む物質を使っていたが、臨床研究には適さない。一方、こうした物質を使わない方法では細胞を大量に培養するのが難しかった。
そこで高橋教授らは、動物由来成分を含まず細胞を安定させる効果を持つ物質「合成ラミニン」を使用。安全性を確保しつつ、iPS細胞から大量の神経細胞を作ることに成功した。従来の手法と比べ、20倍以上の神経細胞を得ることができたという。
また、iPS細胞から臓器や組織の細胞を作って移植する場合、分化しないまま残った細胞が混入していると体内で腫瘍になるおそれがある。そこで高橋教授らは、細胞の表面にあるタンパク質を認識する抗体を利用して細胞を選別する技術を開発。余分な細胞を取り除くことで、より安全性を向上させた。
実際に神経細胞を脳に移植する手術は開頭を必要とせず、細い針を脳内に差し込んで細胞を注入する。術後も磁気共鳴画像装置(MRI)などで経過観察を続け、万が一にも腫瘍が発生すれば、放射線治療や外科手術で対応するとしている。
■「再生医療元年に」
新たな万能細胞として期待されたSTAP細胞は、その存在自体が疑われる状況に陥っているが、実は今年は、iPS細胞などによる再生医療の実用化と普及を促進するため、国が積極的に進めてきた法整備が一定整う大きな1年だ。
日本再生医療学会の岡野光夫(てるお)理事長は「『再生医療元年』になるだろう」と意気込む。
昨年5月、再生医療の基本理念を定めた「再生医療推進法」が施行。同11月に成立した「再生医療安全性確保法」と「改正薬事法」は、今秋に施行される。
安全性確保法は、再生医療のルールを明確にすることで、安全性を確保しながら迅速な普及を図るのが目的。改正薬事法は、これまで医薬品と医療機器に分かれていた承認の仕組みに新しく「再生医療製品」を加え、実用化にかかる時間を短縮するものだ。
安全性確保法によると、iPS細胞を使った臨床研究は、まず大学などに置かれる「特定認定委員会」が審査。この後、計画の提出を受けた厚生労働省が90日以内に安全性を確認し、問題がなければ臨床研究のスタートとなる。厚労省は今年6月ごろ特定認定委の設置基準を示す。
こうした流れを受け、優れた研究成果を臨床の現場で実際に患者の治療につなげるため、同学会は「再生医療認定医」と「臨床培養士」の認定制度を創設することを決定。あわせて、再生医療で健康被害が出た場合の補償に備える保険制度を整備する方針だ。
認定医制度は再生医療について一定の知識や経験を持つ医師が対象で、医療倫理や法制度などの講習を受けることを義務づける。臨床培養士制度は、再生医療で重要となる安全で良質な細胞培養の専門家を、筆記と実技の試験で認定する。保険制度は、損保業界と連携して今秋には制度を整えたいという。
■“夢の医療”実現へ
CiRAでは、iPS細胞を使って輸血用血小板の供給を目指している江藤浩之教授のグループも、近く臨床研究を予定している。江藤教授らは来年中にも臨床研究を申請。平成28年には江藤教授らが設立したベンチャー企業「メガカリオン」が日米で治験を始める計画で、米国では6年後、国内で10年後をめどに実用化したい考えだ。
同社は今年3月、京大付属病院の先端医療機器開発・臨床研究センター内にクリーンルームを設置。広さは約120平方メートルで、培養機器や冷凍庫などが置かれた培養室はほぼ無菌状態に管理されている。iPS細胞から安全かつ大量に血小板の細胞を作製することができるという。
体中のさまざまな臓器や組織になる能力を持ち、ほぼ無限に増殖できるiPS細胞。同分野であるSTAP細胞研究を巡って勃発した一連の騒動がCiRA関係者にとっても気にならないはずはないが、“夢の医療”の実現へ向けた地道な歩みを一歩一歩積み重ねている。
|
|
|
|
|
|
 スパムメールの中から見つけ出すためにメールのタイトルには必ず「阿修羅さんへ」と記述してください。
スパムメールの中から見つけ出すためにメールのタイトルには必ず「阿修羅さんへ」と記述してください。すべてのページの引用、転載、リンクを許可します。確認メールは不要です。引用元リンクを表示してください。